Categorias:

ANVISA – Consulta Dirigida sobre a CP Nº 703/2019 que dispõe sobre a regulamentação de Medicamentos Radiofármacos no Brasil
No último dia 20 de Abril a ANVISA disponibilizou em sua página na Internet a Consulta Dirigida [...]
Ler mais
ANVISA aprova o primeiro produto à base de Cannabis
Foi publicado no DOU do dia 22 de Abril a autorização sanitária do primeiro produto à base de [...]
Ler mais
ANVISA otimiza fluxo de análise de petições de bula e rotulagem para pós-registro de Inclusão de Nova Concentração
A ANVISA aprimorou o fluxo de análise de bula e rotulagem de petições pós-registro relacionadas [...]
Ler mais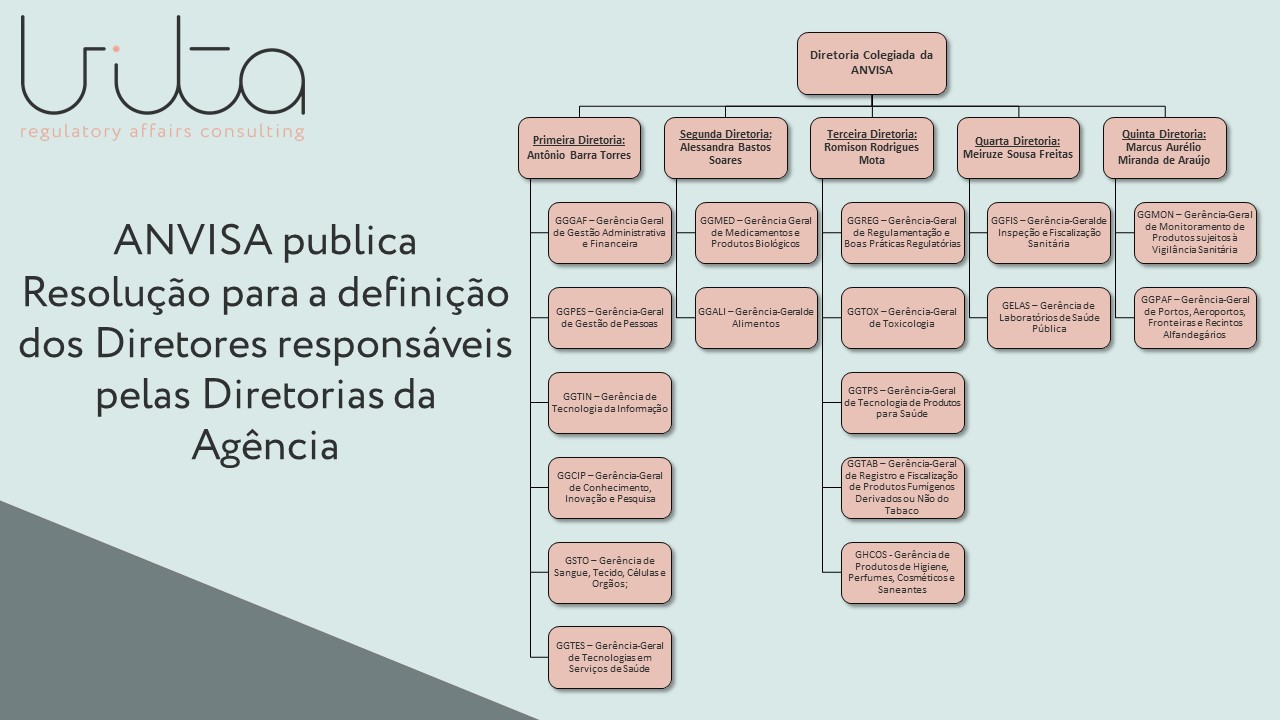
ANVISA publica Resolução para a definição dos Diretores responsáveis pelas Diretorias da Agência
Em 09/04/2020 foi publicado no Diário Oficial da União, a Resolução – RDC Nº 369, de 8 de [...]
Ler mais
ANVISA – Novo Marco Regulatório de Insumos Farmacêuticos Ativos no Brasil
Após um longo trabalho da ANVISA e do setor regulado na discussão das novas diretrizes para o [...]
Ler mais
ANVISA publica Resolução que altera a RDC Nº 304/2019, que dispõe sobre Boas Práticas de Distribuição, Armazenagem e de Transporte de Medicamentos
A ANVISA publicou no Diário Oficial da União a RDC Nº 360, de 27 de Março de 2020 que altera a [...]
Ler mais
ANVISA cria mecanismos alternativos temporários em virtude da pandemia do COVID-19 (última atualização em 09/09/2020)
No dia 13 de Março, a ANVISA publicou no DOU a RDC N° 346, de 12 de Março de 2020, que define [...]
Ler mais
ANVISA – Orientação de Serviço Nº 72/2019 referente à rotulagem de medicamentos registrados e notificados.
A Agência Nacional de Vigilância Sanitária publicou no dia 17 de Outubro de 2019, a Orientação [...]
Ler mais
ANVISA – Sistema Solicita permite aditamento por empresas terceiras
A ANVISA informa que o Sistema Solicita agora permite o aditamento por terceiros. A nova [...]
Ler mais
ANVISA – Aditamentos do CTD já estão disponíveis
A ANVISA informa que o peticionamento dos aditamentos do CTD (Commom Technical Document), [...]
Ler mais
ANVISA – Edital de Chamamento Público para similares que ainda não tiveram a adequação à RDC nº 134/2003 avaliada pela ANVISA – atualizado em 19/02/2020
A Anvisa emite a Orientação de Serviço N° 79/GGMED/DIRE2/ANVISA, de 29 de Janeiro de 2020 e [...]
Ler mais
ANVISA – Entenda a nova Norma que amplia a validade de registro dos medicamentos para 10 anos
Hoje, dia 21 de janeiro de 2020, entra em vigor a Resolução da Diretoria Colegiada – RDC [...]
Ler mais
